Valse meeldauw wordt veroorzaakt door de oomycete Plasmopara viticola en zorgt voor grote problemen in wijngaarden over de hele wereld. Om infectie te bereiken, moet P. viticola de afweermechanismen van de plant overwinnen. Er is daarvoor een echte evolutionaire strijd gaande tussen P.viticola en de wijnstok. Hun complexe samenspel wordt de afgelopen jaren langzaam ontrafeld, maar er is nog een lange weg te gaan.
De wijnstok heeft, zoals alle planten, in de loop van de evolutie een complex afweermechanisme tegen micro-organismen ontwikkeld. Dit aangeboren immuunsysteem detecteert potentiële indringers. In reactie op schade of omgevingsstress begint de plant hormonen te produceren zoals jasmijnzuur, salicylzuur en ethyleen die verschillende afweerreacties in gang zetten, zoals de productie van reactieve zuurstofradicalen (ROS) en fytoalexines, het sluiten van de huidmondjes, of de afzetting van callose om de celwand te versterken. De aanvalsmechanismen van micro-organismen zoals P. viticola worden echter ook constant verbeterd, waardoor een evolutionaire wapenwedloop tussen pathogenen en planten is ontstaan.
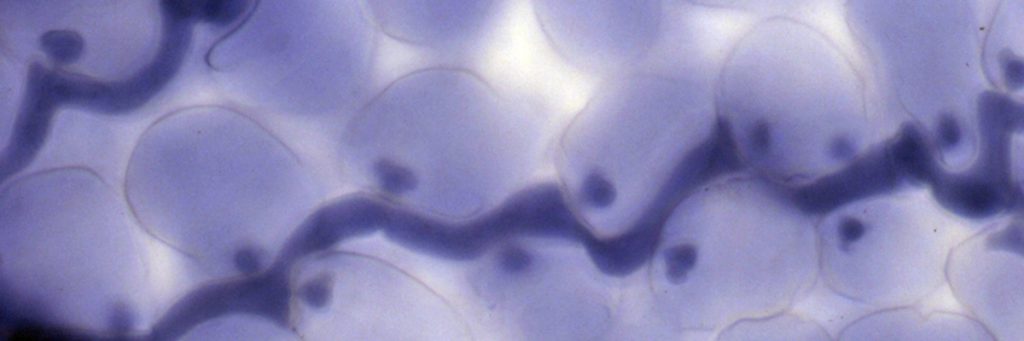
Valse meeldauw schimmeldraad met haustoria (bolletjes in de cellen) groeiend in het blad van Arabidopsis thaliana, waargenomen met behulp van bright-field microscopy.
Aangepast van Emmanuel Boutet via CC BY-SA 2.5
Parasiet
Oomyceten zoals P. viticola hebben water nodig om te ontkiemen en worden daarom vaak ‘waterschimmels’ genoemd. Tijdens regen spatten zoösporen van P. viticola op de bladeren van de wijnstok en zwemmen naar de huidmondjes. Vervolgens komt de kiembuis van de zoöspore in het huidmondje en vormt een schimmeldraad (ook wel hypha genoemd) in het blad. De schimmeldraad is een lange vertakte structuur die zich verder uitstrekt in het blad van de wijnstok en haustoria vormt in de cellen. Deze haustoria zijn zuigorganen die door de celwand van de plant dringen waardoor P. viticola voedingsstoffen uit de cel kan opzuigen en kan gebruiken om te groeien. Amerikaanse druivensoorten kunnen dit parasitaire gedrag blokkeren door de aangetaste cellen geprogrammeerd dood te laten gaan. Vitis vinifera-soorten kunnen dit niet en zijn daarom kwetsbaarder voor P. viticola1,2.
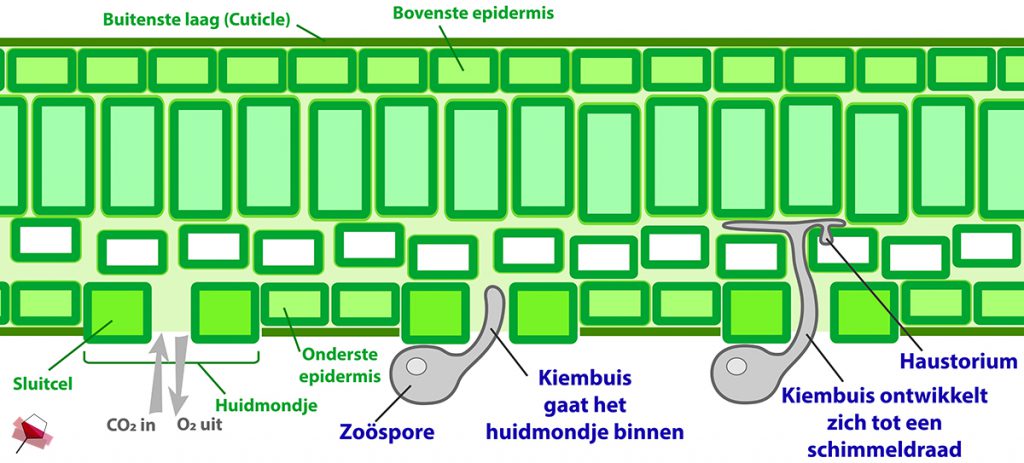
Dwarsdoorsnede van een wijnblad. Infectie van het blad door P. viticola zoöspore en de vorming van schimmeldraden en een haustorium
Evolutionaire wapenwedloop
Bij een aanval door micro-organismen is de eerste actie van het immuunsysteem van de wijnstok het detecteren van pathogeen-geassocieerde moleculaire patronen (PAMP’s). Deze PAMPs zijn (delen van) moleculen die typisch zijn voor microben en niet geassocieerd worden met de eigen cellen van de plant. Voorbeelden hiervan zijn lipopolysaccharide voor gramnegatieve bacteriën, dubbelstrengs RNA voor virussen, en β-glucanen die worden aangetroffen in celwanden van schimmels. Wanneer deze moleculen door de plant worden herkend, wordt het immuunsysteem geactiveerd. Deze immuunrespons wordt de ‘PAMP-triggered immunity’ (PTI) genoemd en wordt gereguleerd door de eerdergenoemde planthormonen.
Tijdens de evolutie hebben pathogenen zoals P. viticola zich aangepast om de PTI te omzeilen door ‘effectoren’ af te scheiden. Effectoren zijn gespecialiseerde eiwitten die de gevoeligheid van de plant voor de ziekteverwekker vergroten. Dit proces wordt de ‘effector-triggered susceptibility’ (ETS) genoemd en verhoogt de virulentie van de ziekteverwekker. Maar zoals bij alle evolutieprocessen, heeft de plant zich hier ook op aangepast en heeft ze manieren ontwikkeld om de effectoren te herkennen met behulp van resistentie-eiwitten. Activering van deze eiwitten in de plantencel leidt tot een immuunrespons die ‘effector-triggered immunity’ (ETI) wordt genoemd. De afweerreacties van de ETI zijn vergelijkbaar met die van de PTI, maar zijn vaak intenser, wat resulteert in celdood op de plaats van de infectie. Deze geprogrammeerde celdood is een afweermechanisme van de plant om de groei van P. viticola te stoppen en wordt ook wel de ‘overgevoelige reactie’ (hypersensitive response) genoemd.
Pathogenen en planten verbeteren en ontwikkelen voortdurend nieuwe mechanismen van ETS en ETI, wat resulteert in een evolutionaire wapenwedloop2-4.
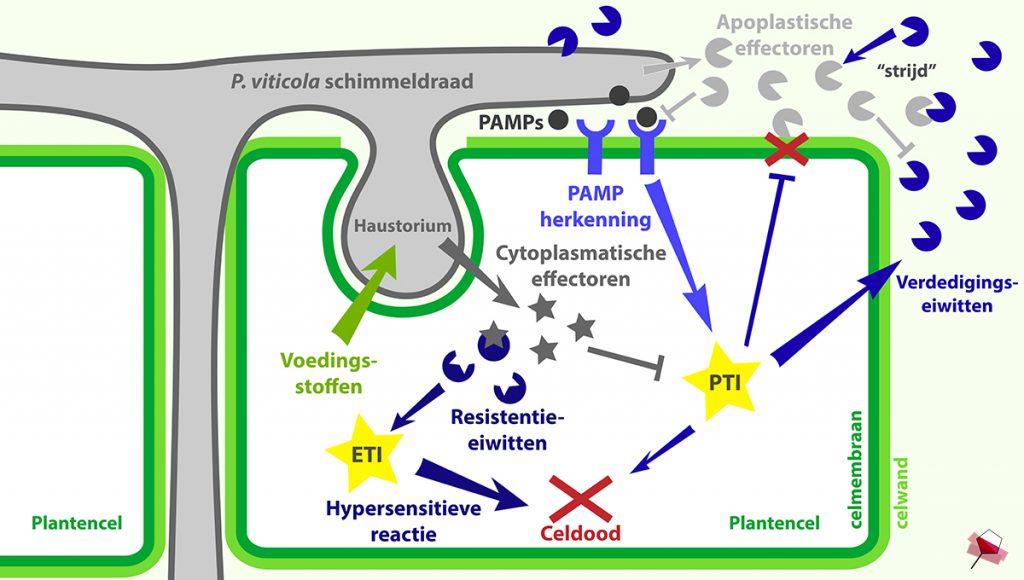
Interactie tussen de door P. viticola geproduceerde effectoren en het immuunsysteem van de plantencel.
EFFECTOREN
P. viticola-isolaten uit Italië, Frankrijk en China zijn gekarakteriseerd en bleken verschillende sets effectoren te produceren3. Deze effectoren zijn kandidaat-effectoren omdat ze geïdentificeerd zijn op basis van hun geconserveerde domein, en niet functioneel zijn bestudeerd. Voor een aantal families van de kandidaat-effectoren van P. viticola zijn al studies verricht naar hun functie en subcellulaire lokalisatie5,6, maar er is nog een lange weg te gaan.
Desalniettemin bestaat er een goed algemeen idee over hoe de verschillende families van effectoren bijdragen aan de virulentie van P. viticola. Dat wil zeggen, de geproduceerde effectoren kunnen in de plantencel worden getransporteerd, waar ze de immuunafweer van de planten verzwakken door het verstoren van de planthormonen7. Maar daarnaast zijn er ook effectoren die hun functie op de buitenkant van de plantencel uitoefenen. Ze beschadigen de celwand en het celmembraan, of verstoren de werking van receptoren en/of de verdedigingseiwitten van de plantencel. De groep effectoren die de cel in gaan zijn de cytoplasmatische effectoren, en de effectoren die buiten de cel hun werk doen worden apoplastische effectoren genoemd.

Valse meeldauw op het blad van een wijnstok.
Aangepast van Rude via CC BY-SA 3.0
Cytoplasmatische effectoren
Er zijn drie overheersende families van cytoplasmatische effector-eiwitten geïdentificeerd in P.viticola. Dit zijn de RXLR-effector-eiwitten, de CRN-effector-eiwitten en de YxSLK-effector-eiwitten2. De eiwitten in deze families worden gekenmerkt door een geconserveerd domein. De RXLR-eiwitten hebben bijvoorbeeld een RXLR-domein dat bestaat uit een geconserveerd Arginine (R), willekeurig aminozuur (X), Leucine (L) en Arginine (R) motief. Deze domeinen zijn vereist voor het binnenkomen van het effectoreiwit in de plantencel en zorgen er voor dat de effectoren getransporteerd worden naar specifieke subcellulaire locaties zoals de kern, het cytosol, het membraan of zelfs de chloroplasten en mitochondriën in de cel5. Onderzoekers gebruiken dit geconserveerde domein ook om nieuwe vermeende cytoplasmatische effectoren in het transcriptoom van P.viticola te herkennen2,3. Eenmaal in de cel oefent de rest van het eiwit vervolgens zijn effecten uit om afweerreacties zoals de PTI te onderdrukken en de virulentie van de ziekteverwekker te bevorderen2-4.
Een interessant gegeven is dat veel resistentie-eiwitten het vermogen hebben om RXLR-motieven te herkennen. Eiwitten van de familie van RXLR-effectoren zijn daarom vaak belangrijk voor de resistentie van de plant tegen P. viticola. Als zodanig zijn veel RXLR-effectoren contraproductief en belemmeren ze de infectie en worden daarom ook wel avirulentiefactoren genoemd8,9.
Apoplastische effectoren
Apoplastische effectoren komen niet in de cel, maar interageren met extracellulaire eiwitten en receptoren op het oppervlak van de plantencel om de infectie te bevorderen. De meest voorkomende apoplastische effectoren zijn glycosidehydrolasen, proteases en proteaseremmers, maar extracellulaire toxines zoals NLP’s en degradatieve enzymen zoals cellulasen, cutinasen, pectaatlysasen en pectine-esterasen worden ook tot expressie gebracht door P. viticola3. De degradatieve enzymen richten zich op verschillende componenten van de celwand en het membraan van de plant om afbraak en penetratie van de cel mogelijk te maken.
De verscheidenheid van deze effectoren toont de complexiteit van de interactie tussen pathogeen en plantencel. De proteaseremmers die tot expressie worden gebracht door P. viticola, richten zich bijvoorbeeld op de proteasen die worden uitgescheiden door de wijnstok, die opnieuw werden geproduceerd om de effectoren die werden uitgescheiden door P. viticola af te breken.
Een overzicht van al deze families van (cytoplasmatische en apoplastische) effectoren die bekend zijn voor P. viticola is weergegeven in Tabel 1.
Tabel 1. Effectors die worden geproduceerd door Plasmopara viticola om te helpen bij de infectie van de druivenstok2-4,6
| Cytoplasmatische effectoren | Functie |
| RXLR effectoren | Verstoren en remmen de PTI en andere afweerreacties van planten in de plantencel |
| CRN effectoren | Verstoren en remmen de PTI en andere afweerreacties van planten in de plantencel |
| YxSLK effectoren | Verstoren en remmen de PTI en andere afweerreacties van planten in de plantencel |
| Apoplastische effectoren | Functie |
| Cellulasen | Afbraak van cellulose in de celwand |
| Cutinasen | Afbraak van cutine, een polymeer dat het oppervlak van het blad beschermt. |
| Elicitin-achtige eiwitten | Een giftig eiwit dat necrose en een overgevoeligheidsreactie veroorzaakt. Verzamelt sterolen uit de plantencel. |
| Trypsin-achtige eiwitten | Proteasen die eiwitten splitsen. Betrokken bij het reactiemechanisme tegen afweer van planten. |
| Glycosidehydrolasen | Brede familie van eiwitten die betrokken zijn bij de hydrolyse (afbraak) van glycosidebindingen. |
| Lipasen | Afbraak van lipiden. |
| NLPs | NLP’s induceren necrose en de ethyleenreactie in plantencellen. Mogelijk ook betrokken bij de hechting van zoosporen en het onderdrukken van PAMP-herkenning. |
| Pectine-esterasen | Afbraak van de plantencelwand |
| Pectaatlyases | Klieft pectinezuur, een afbraakproduct van pectine. |
| Proteases | Afbraak van eiwitten (ook wel ‘peptidasen’ genoemd) |
| Proteaseremmers | Blokkeren de afbraak van eiwitten door proteasen te remmen |
Identificatie van resistentiegenen
De grote verschillen in gevoeligheid bij Vitis-soorten zijn te wijten aan het feit dat P. viticola afkomstig is uit Noord-Amerika. In de jaren 1870 werd P. viticola in Europa geïntroduceerd waardoor valse meeldauw zorgde voor enorme schade aan de Europese wijngaarden. De Europese Vitis vinifera druivenrassen bleken zeer vatbaar te zijn voor valse meeldauw, in tegenstelling tot de Noord-Amerikaanse Vitis-soorten die door co-evolutie een natuurlijke weerstand hadden opgebouwd. Amerikaanse Vitis-soorten brengen daarom een set resistentie-eiwitten tot expressie die niet worden geproduceerd in de Vitis vinifera-variëteiten. Er is grote belangstelling voor de genen die voor deze resistentie-eiwitten coderen, omdat ze zorgen voor de benodigde resistentie tegen P. viticola. Daarnaast is het ook mogelijk dat vatbare wijnstokken juist genen hebben die niet aanwezig zijn in de Amerikaanse druiven, en zorgen voor een verhoogde gevoeligheid voor valse meeldauw. Om al deze genen te ontdekken, wordt de interactie tussen P. viticola met gevoelige en resistente Vitis-soorten bestudeerd en worden hun transcriptomen vergeleken.
Toffolatti en collega’s vergeleken het transcriptoom van de gevoelige Pinot noir met dat van de resistente hybride Bianca en het resistente Vitis vinifera druivenras Mgaloblishvili. Deze laatste is een druivenras uit Georgië dat unieke resistentiekenmerken vertoont. Ze vonden een gevoeligheidsgen en een grote lijst van nieuwe kandidaatgenen die resistentie zouden kunnen verlenen tegen P. viticola2. De functie van de meeste van deze transcripten is echter onbekend en er zullen functionele tests moeten worden uitgevoerd om te bepalen of, en hoe deze genen bijdragen aan de resistentie tegen P. viticola.
Kweek van resistente druivenrassen
Kennis over de exacte mechanismen die de immuunresponse tegen P. viticola reguleren zou de (moleculaire) veredeling van nieuwe resistente wijnstokrassen ten goede komen. Nieuwe variëteiten kunnen dan worden geselecteerd op basis van hun vermogen om resistentie-eiwitten tot expressie te brengen, waardoor het selectieproces wordt verkort.
LEES OOK: Veredeling, genetische modificatie en gene-editing in de wijngaard
Als alternatief kunnen nieuw ontwikkelde druivenrassen ook onderworpen worden aan een set effectoren waarvan bekend is dat ze de ETI in resistente rassen activeren. Brilli en collega’s toonden bijvoorbeeld aan dat de RXLR-effector genaamd PVITv1008311 de ETI in de Amerikaanse Vitis riparia activeert. Dit resulteerde in necrotische vlekken op de bladeren en een verminderde groei van P. viticola. Deze zelfde effector veroorzaakte geen immuunreactie bij de gevoelige Pinot noir-druif. Dit laat zien dat, hoewel de exacte immuunrespons die door deze effector bij Vitis riparia wordt veroorzaakt nog niet bekend is, hij wel kan worden gebruikt om te screenen op nieuwe resistente druivenrassen10.
Toekomstig onderzoek
Het samenspel tussen P. viticola en de wijnstok is complex en bestaat uit meerdere lagen van virulentie en afweermechanismen. Toekomstig onderzoek zal waarschijnlijk aantonen dat deze evolutionaire strijd zelfs nog complexer is dan we al weten, maar zal veredelaars ook de juiste instrumenten geven om nieuwe resistente rassen te ontwerpen en te produceren. Bovendien, wanneer de immuunmechanismen bekend zijn, is het ook mogelijk om alternatieven te ontwikkelen voor koper en schadelijke chemische bestrijdingsmiddelen waarmee valse meeldauw effectief kan worden bestreden.
Referenties
1. Toffolatti SL, De Lorenzis G, Costa A, Maddalena G, Passera A, et al. Unique resistance traits against downy mildew from the center of origin of grapevine (Vitis vinifera). Sci Rep. 2018 Aug 21;8(1):12523. https://doi.org/10.1038/s41598-018-30413-w.
2. Toffolatti SL, De Lorenzis G, Brilli M, Moser M, Shariati V, et al. Novel Aspects on The Interaction Between Grapevine and Plasmopara viticola: Dual-RNA-Seq Analysis Highlights Gene Expression Dynamics in The Pathogen and The Plant During The Battle For Infection. Genes (Basel). 2020 Feb 28;11(3). pii: E261. doi: https://doi.org/10.3390/genes11030261.
3. Yin L, Li X, Xiang J, Qu J, Zhang Y, et al. Characterization of the secretome of Plasmopara viticola by de novo transcriptome analysis. Physiological and Molecular Plant Pathology. 2015 July;91:1-10. https://doi.org/10.1016/j.pmpp.2015.05.002
4. Jiang RHY and Tyler BM. Mechanisms and Evolution of Virulence in Oomycetes. Annu. Rev. Phytopathol. 2012 50:295-318. https://doi.org/10.1146/annurev-phyto-081211-172912
5. Liu Y, Lan X, Song S, Yin L, Dry IB, Qu J, Xiang J, Lu J. In Planta Functional Analysis and Subcellular Localization of the Oomycete Pathogen Plasmopara viticola Candidate RXLR Effector Repertoire. Front Plant Sci. 2018 Apr 13;9:286. https://doi.org/10.3389/fpls.2018.00286. eCollection 2018.
6. Schumacher S, Grosser K, Voegele RT, Kassemeyer HH, Fuchs R. Identification and Characterization of Nep1-Like Proteins From the Grapevine Downy Mildew Pathogen Plasmopara viticola. Front Plant Sci. 2020 Feb 13;11:65. https://doi.org/10.3389/fpls.2020.00065. eCollection 2020.
7. Han X, Kahmann R. Manipulation of Phytohormone Pathways by Effectors of Filamentous Plant Pathogens. Front Plant Sci. 2019 Jun 26;10:822. https://doi.org/10.3389/fpls.2019.00822. eCollection 2019.
8. Mestre P, Carrere S, Gouzy J, Piron M-C, Tourvieille de Labrouhe D, et al. Comparative analysis of expressed CRN and RXLR effectors from two Plasmopara species causing grapevine and sunflower downy mildew. Plant Pathology. 2015 Oct 11;65(5):767-781. https://doi.org/10.1111/ppa.12469
9. Amaro TM, Thilliez GJ, Motion GB, Huitema E. A Perspective on CRN Proteins in the Genomics Age: Evolution, Classification, Delivery and Function Revisited. Front Plant Sci. 2017 Feb 3;8:99. https://doi.org/10.3389/fpls.2017.00099. eCollection 2017.
10. Brilli M, Asquini E, Moser M, Bianchedi PL, Perazzolli M, Si-Ammour A. A multi-omics study of the grapevine-downy mildew (Plasmopara viticola) pathosystem unveils a complex protein coding- and noncoding-based arms race during infection. Sci Rep. 2018 Jan 15;8(1):757. https://doi.org/10.1038/s41598-018-19158-8.
hallo daar
aakan u ons ook vertellen hoe we dat kunnen bestrijden?
vast bedankt
Willem schouten
Canada